
A ministra interina da Ciência e Tecnologia, Emília Curi, afirmou nesta quinta-feira (14) que teria pedido “um prazo maior” antes de liberar a substância fosfoetanolamina sintética — conhecida como a pílula do câncer. Nesta quarta, a presidente Dilma Rousseff sancionou a lei que autoriza o uso do composto por pacientes diagnosticados com tumores malignos.
“Como pesquisadora, como cientista do Ministério da Ciência e Tecnologia, nós teríamos pedido um prazo ao Congresso Nacional, como nós pedimos, que esperasse um amadurecimento das pesquisas”, disse a chefe da pasta.
Por outro lado, ela disse que o ministério é responsável apenas pela condução de pesquisas e que a sanção da lei responde a uma “comoção da sociedade”. “Não é um assunto que está sendo discutido hoje. Está sendo discutido há muitos anos, debatido há muito tempo. Não há nenhuma precipitação com relação ao tema.”
A pasta informou que já liberou R$ 2 milhões para pesquisas que estão sendo conduzidas com o objetivo de testar a eficiência da fosfoetanolamina. Segundo o secretário de Programas e Políticas de Pesquisa e Desenvolvimento, Jailson de Andrade, o órgão pode liberar até R$ 10 milhões para análises.
“Até o momento, os estudos in vitro [iniciais] mostram, que ela não é toxica nas doses que foram estudadas, mas não mostraram nenhuma atividade com relação ao combate ao câncer”, continuou o secretário. “Não tem evidencias seguras que atue em relação ao que se propõe, em relação ao combate ao câncer. A garantia é que não está sendo liberado nada que é tóxico.”
De acordo com o órgão, a previsão é de que os estudos iniciais sejam concluídos até o início do segundo semestre para então poderem ser realizados testes mais avançados, como administração em seres humanos. O ministério não deu estimativa de quando será possível concluir se a fosfoetanolamina é segura e eficiente.
Substância aprovada
A sanção da lei número 13.269, de 13 de abril de 2016, foi publicada no Diário Oficial da União desta quinta-feira. O artigo 1º destaca que “esta lei autoriza o uso da substância fosfoetanolamina sintética por pacientes diagnosticados com neoplasia maligna”.
O artigo 2º ressalta que só “poderão fazer uso da fosfoetanolamina sintética, por livre escolha”, os pacientes que apresentarem “laudo médico que comprove o diagnóstico” e “assinatura de termo de consentimento e responsabilidade pelo paciente ou seu representante legal”.
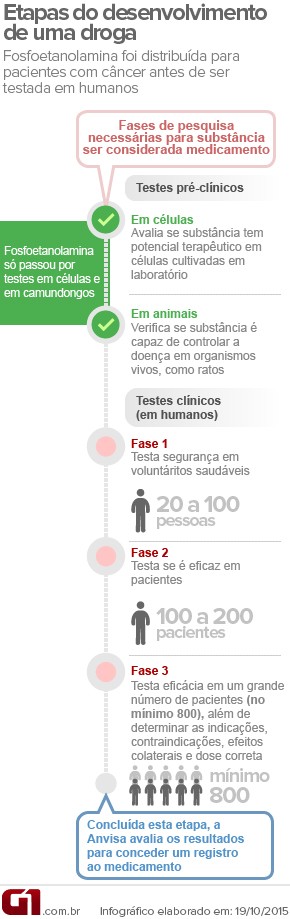
Distribuída pela Universidade de São Paulo em São Carlos até suspensão determinada pelo Supremo Tribunal Federal (STF), a fosfoetanolamina é alardeada como cura para diversos tipos de câncer, mas não passou por testes em humanos e, por isso, não é considerada um remédio. Ela não tem registro na Anvisa e seus efeitos nos pacientes são desconhecidos.
Os primeiros relatórios sobre as pesquisas financiadas pelo governo federal apontaram que as cápsulas têm uma concentração de fosfoetanolamina menor do que era esperado e que somente um dos componentes da cápsula – a monoetanolamina – apresentou atividade citotóxica e antiproliferativa, ou seja, capacidade de destruir células tumorais e inibir seu crescimento.
Críticas à liberação
A Associação da Indústria Farmacêutica de Pesquisa (Interfarma), que reúne 56 laboratórios que são responsáveis por 82% dos medicamentos de referência disponíveis no mercado, criticou duramente a sanção da lei:
“O Brasil, a partir de hoje, entra na história da ciência mundial e da indústria farmacêutica como o primeiro país a legalizar a irresponsabilidade, anular a importância da ciência e a igualar o remédio com o não remédio. Uma decisão tão sem sentido que informa que a droga, que não foi testada nem aprovada pela Anvisa, só pode ser produzida por quem tem autorização para fabricação de medicamentos pela mesma Anvisa.”
A agência de vigilância divulgou uma nota dizendo que vê a liberação da substância com “uma preocupação profunda”. “Cria-se uma situação de exceção em que pessoas poderão estar expostas a diversos riscos sanitários”, afirmou o órgão.
Aprovação no Congresso
A lei sancionada pela presidente foi aprovada pelo Senado no dia 22 de março, em votação simbólica. Como não houve alterações ao texto aprovado pela Câmara dos Deputados, o projeto seguiu para a sanção presidencial.
“Ficam permitidas a produção e manufatura, importação, distribuição e prescrição, dispensação, posse ou uso da fosfoetanolamina sintética, direcionadas aos usos de que trata esta lei, independentemente de registro sanitário, em caráter excepcional, enquanto estiverem em curso estudos clínicos acerca dessa substância”, diz o texto da lei.
O projeto ressalva, porém, que a produção da “pílula do câncer” só pode ser feita por “agentes regularmente autorizados e licenciados pela autoridade sanitária competente”.
Surgimento da pílula
A fosfoetanolamina sintética começou a ser estudada no Instituto de Química da USP em São Carlos, pelo pesquisador Gilberto Chierice, hoje aposentado. Apesar de não ter sido testada cientificamente em seres humanos, as cápsulas foram entregues de graça a pacientes com câncer por mais de 20 anos.
Em junho do ano passado, a USP interrompeu a distribuição e os pacientes começaram a recorrer da decisão na Justiça. Em outubro deste ano, a briga foi parar no Supremo Tribunal Federal (STF), que autorizou a produção e distribuição do produto.
Por uma nova decisão judicial, a distribuição da substância estava proibida desde novembro. A polícia chegou a fechar um laboratório em Conchal (SP), que estava produzindo ilegalmente a substância.
A USP tinha fechado no dia 1º de abril o laboratório de São Carlos que produzia a fosfoetanolamina sintética.



